Kalor merupakan bentuk energi yang pindah karena adanya perbedaan suhu.
Secara alamiah, kalor berpindah dari benda bersuhu tinggi ke benda
bersuhu rendah. Sebelum abad ke – 17, orang beranggapan bahwa kalor
merupakan zat yang pindah dari benda bersuhu tinggi ke benda yang
bersuhu rendah. Jika kalor merupakan zat, tentu mempunyai masa. Ternyata
benda yang suhunya naik, massanya tidak berubah, jadi kalor bukan zat.Satuan kalor :
Sistem internasional ( SI ) ; joule ( J )
Sistem lain ; kalori ( kal ) dimana 1 kalori = 4,2 ; BTU dimana 1 BTU = 252 kalor
Sistem internasional ( SI ) ; joule ( J )
Sistem lain ; kalori ( kal ) dimana 1 kalori = 4,2 ; BTU dimana 1 BTU = 252 kalor
Jumlah
kalor yang diperlukan/dilepaskan untuk menaikkan/menurunkan suhu suatu
benda sebanding dengan massa benda dan bergantung pada jenis zat itu.Secara matematis dirumuskan sebagai berikut:
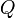 adalah banyaknya kalor (jumlah panas) dalam joule
adalah banyaknya kalor (jumlah panas) dalam joule adalah massa benda dalam kg
adalah massa benda dalam kg adalah kalor jenis dalam joule/kg °C, dan
adalah kalor jenis dalam joule/kg °C, dan adalah besarnya perubahan suhu dalam °C.
adalah besarnya perubahan suhu dalam °C.
Kalor dapat menyebabkan perubahan wujud, seperti berikut ini:

1) Peleburan, proses perubahan zat cair menjadi zat padat.
2) Pembekuan, proses perubahan zat padat menjadi zat cair.
3) Penguapan, proses perubahan zat cair menjadi gas.
4) Pengembunan, proses perubahan gas menjadi zat cair.
5) Pengkristalan/deposisi, proses perubahan gas menjadi zat padat.
6) Penyumbliman, proses perubahan zat padat menjadi gas.
Kalor laten adalah kalor yang diperlukan untuk mengubah wujud zat tanpa
kenaikan suhu tiap satuan massa. Kalor laten terdiri dari kalor
lebur/beku dan kalor uap/embun.
Energi kalor yang dihasilkan kalor laten dapat dirumuskan:
Q = m L
Keterangan:
Q= kalor (J)
m=massa (kg)
L= Kalor Laten (J/kg)
Pada perubahan wujud air dari es menjadi uap, terjadi peleburan dan penguapan.
a. Penguapan air terjadi di permukaan air pada suhu sembarang.
b. Mendidih adalah peristiwa penguapan di seluruh bagian air, terjadi pada suhu 100 derajarat Celcius pada tekanan 1 atm.
c. Tekanan mempengaruhi titik didih dan titik beku air

Perubahan suhu
Jumlah energi panas,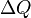 , dibutuhkan untuk menggantu suhu suatu material dari suhu awal, T0, ke suhu akhir, Tf tergantung dari kapasitas panas bahan tersebut menurut hubungan:
, dibutuhkan untuk menggantu suhu suatu material dari suhu awal, T0, ke suhu akhir, Tf tergantung dari kapasitas panas bahan tersebut menurut hubungan:Kapasitas panas molar dapat "dimodifikasi" bila perubahan suhu terjadi pada volume tetap atau tekanan tetap. Bila tidak, menggunakan hukum pertama termodinamika dikombinasikan dengan persamaan yang menghubungkan energi internal gas tersebut terhadap suhunya.
Sumber:
http://id.wikipedia.org/wiki/Panas
https://materi78.files.wordpress.com/2012/10/kalor_fis1.pdf


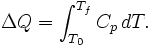
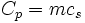

Tidak ada komentar:
Posting Komentar